Wenn die Diagnose Prostatakrebs feststeht und Ausmaß sowie Stadium der Erkrankung bestimmt worden sind, entscheidet der Arzt gemeinsam mit dem Patienten, welche Möglichkeiten der Behandlung genutzt werden. Hier finden Sie Informationen zu folgenden Behandlungsmethoden im Frühstadium:
Abwarten
Das Prostatakarzinom gehört zu den Krebsarten, die häufig nur langsam wachsen und nicht immer eine unmittelbare Bedrohung für die Betroffenen darstellen. Außerdem werden immer mehr Tumoren in einem sehr frühen Stadium entdeckt, so dass möglicherweise eine Therapie eingeleitet wird, obwohl das Karzinom niemals Probleme bereitet hätte. Es muss also abgewogen werden, ob der Nutzen einer Behandlung in einem sinnvollen Verhältnis zu ihren Risiken und zu erwartenden Nebenwirkungen steht. Daher haben abwartende Strategien beim Prostatakarzinom einen wichtigen Stellenwert. Man unterscheidet dabei zwei verschiedene Vorgehensweise: das abwartende Beobachten („Watchful Waiting“) und die aktive Überwachung („Active Surveillance“).
Abwartendes Beobachten
Beim abwartenden Beobachten wird der Tumor vorerst nicht therapiert – unabhängig vom Tumorstadium. Die – palliative – Behandlung beginnt erst und auch nur, wenn Symptome auftreten. Bei Patienten, deren Tumor potenziell geheilt werden könnte, sollte nur dann abgewartet werden, wenn ihre Lebenserwartung aufgrund des Alters oder anderer Erkrankungen unter zehn Jahren und der Gleason-Score nicht über 7 liegt.
Aktive Überwachung
Bei der aktiven Überwachung („Active Surveillance“) werden die Patienten engmaschig überwacht, um ggf. rechtzeitig eine – kurative – Behandlung einleiten zu können. Bleibt der Tumor unauffällig, wird nicht behandelt. Zeichnet sich aber ein Fortschreiten der Erkrankung ab, erfolgt meist eine radikale Prostatektomie, alternativ eine Bestrahlung. Vor der Entscheidung für die aktive Überwachung sollte eine Bildgebung mittels MRT erfolgen.
Die aktive Überwachung eignet sich auch für jüngere Patienten ohne schwere andere Erkrankungen, die folgende Kriterien erfüllen:
- PSA-Wert ≤ 10 ng/ml
- Gleason-Score ≤ 6
- lokal begrenztes Prostatakarzinom (cT1-2a),
- Tumor in ≤ 2 Stanzen
- Tumorbefall je Stanze ≤ 50%.
Die regelmäßigen Kontrollen umfassen die Bestimmung des PSA-Wertes und eine digital-rektale Untersuchung aller drei Monate. Bleibt der PSA-Wert zwei Jahre lang stabil, kann das Kontrollintervall auf 6 Monate verlängert werden. Zusätzlich soll nach einem halben Jahr eine Kontrollbiopsien vorgenommen werden, in den nächsten drei Jahren alle 12 bis 18 Monate, danach bei stabilem Befund alle drei Jahre.
Die Kriterien für die Beendigung der abwartenden Strategie und den Beginn einer aktiven Therapie sind nicht einheitlich definiert. Hinweise darauf, dass die Erkrankung fortschreitet, geben schnell ansteigende PSA-Werte , verschlechterte Gleason-Scores und höhere Tumoranteile in den Kontrollbiospien. Und natürlich kann sich der Patient auch jederzeit selbst entscheiden, nicht länger abzuwarten, sondern aktiv gegen den Tumor vorzugehen.
Operation
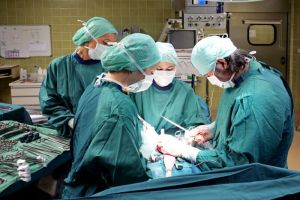
Ist der Krebs auf die Prostata beschränkt, kann er durch eine operative Entfernung der Prostata beseitigt werden. Bei der sogenannten radikalen Prostatektomie werden Prostata und Samenblasen entfernt. Dafür können verschiedene Operationstechniken eingesetzt werden:
- retropubisch: Schnitt im Unterbauch
- perineal: Schnitt durch den Damm (Perineum) zwischen Anus und Peniswurzel
- laparoskopisch: endoskopische Operation durch mehrere Zugänge im Unterbauch (oft Roboter-assistiert)
Die drei Verfahren gelten derzeit als gleichwertig, was den Erfolg der Operation, die Häufigkeit von Komplikationen und die Rate unerwünschter Folgeerscheinungen betrifft.
Mitunter werden während der Operation auch die Lymphknoten im Becken mit entfernt (Lymphadenektomie). Dies geschieht, um bei der mikroskopischen Untersuchung feststellen zu können, wie weit sich die Krankheit ausgebreitet hat und welche weitere Behandlung notwendig ist.
Wie wirksam ist die Operation?
Die Chancen für eine dauerhafte Heilung sind durch eine radikale Prostatektomie sehr gut, insbesondere wenn der Tumor vollständig entfernt werden kann („R0-Resektion“). Je weiter der Krebs allerdings fortgeschritten ist, desto geringer wird die Möglichkeit, eine R0-Resektion zu erreichen und so höher ist entsprechend das Rückfallrisiko.
Welche Folgen hat die Operation?
Trotz der immer weiter verbesserten Operationstechnik lassen sich unerwünschte Folgeerscheinungen der radikalen Prostataentfernung wie Verlust der Erektionsfähigkeit (Impotenz) und ungewolltes Wasserlassen (Harninkontinenz) nicht komplett vermeiden. Wie häufig die genannten Komplikationen auftreten, ist schwer zu sagen, da in den Studien unterschiedliche Operationsmethoden angewendet und verschiedene Tumorstadien untersucht worden, weshalb die Ergebnisse stark voneinander abweichen.
Eine vorübergehende Harninkontinenz ist relativ häufig (gering ausgeprägt: bis zu 50% der Patienten; hochgradig: bis zu 15%). Es dauert in der Regel ein paar Wochen oder Monate, bis die Haltefunktion des Harnröhrenschließmuskels – insbesondere bei Belastung wie Husten oder Niesen – wieder komplett hergestellt ist. Durch ein gezieltes Training, sogenanntes Beckenbodentraining, kann einer langfristigen Inkontinenz erfolgreich entgegengewirkt werden. Zu einer bleibenden Inkontinenz kommt es bei etwa 5 bis 10 Prozent der operierten Patienten.
Die Einschränkung oder der Verlust der Erektionsfähigkeit (erektile Dysfunktion, Impotenz) ist dadurch bedingt, dass bei der Prostataentfernung die Nervenstränge verletzt werden, die für die Erektion verantwortlich sind. Diese Nervenstränge laufen rechts und links an der Prostata entlang. Je nachdem, wie weit sich der Krebs ausgebreitet hat, können ein oder beide Nervenbündel bei der Operation geschont werden. Dennoch können je nach Tumorausbreitung und Erfahrung des Operateurs bis zu 80% der operierten Patienten dauerhaft impotent bleiben.
Seltenere Nebenwirkungen der radikalen Prostatektomie sind narbenbedingte Verengungen des Blasenhalses (Anastomosenstriktur), Verletzungen des Enddarms und Stuhlinkontinenz.
Strahlentherapie
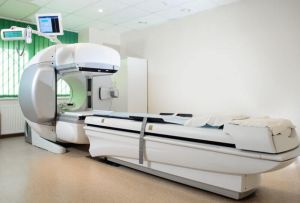
Bei der Strahlentherapie wird mit radioaktiver Strahlung direkt auf den Tumor gezielt. Dadurch werden die Zellkerne der Krebszellen so stark geschädigt, dass die Krebszellen sich nicht mehr teilen können und zu Grunde gehen. Grundsätzlich wird die Strahlentherapie bei lokal begrenzten und lokal fortgeschrittenen Tumoren eingesetzt, bei letzteren in Kombination mit einer unterstützenden (neoadjuvanten) Hormontherapie.
Bei einigen Patienten wird die Strahlentherapie auch als zusätzliche Maßnahme nach der Operation durchgeführt (adjuvante Strahlentherapie). Damit soll das Risiko einer Wiedererkrankung (Rezidiv) vermindert werden.
Es gibt zwei unterschiedliche Arten der Bestrahlung: die von außen (perkutan: lat. „durch die Haut“) und die von innen (Brachytherapie: griech. „kurz, nah“).
Perkutane Strahlentherapie
Bei der perkutanen Strahlentherapie wird der Tumor durch eine außerhalb des Körpers befindliche Strahlenquelle bestrahlt. Es wird empfohlen, die perkutane Strahlentherapie intensitäts-moduliert (d.h. in IMRT-Technik) unter Einsatz bildgeführter Techniken durchzuführen. Zunächst wird dazu die Prostata z. B. mit Hilfe einer Computertomografie abgebildet. Anhand dessen kann genau das Areal bestimmt werden, das von der Strahlung getroffen werden soll.
Die Strahlenquelle wird nun von mehreren Seiten aus genau auf den Tumor gerichtet. Nur dort, wo sich die Strahlen aus den verschiedenen Richtungen überschneiden, wird die wirksame Strahlendosis erreicht; das umliegende gesunde Gewebe wird geschont.
Bestahlt wird über mehrere Wochen mit einer Gesamtdosis von 74 bis <80 Gy (Gray = Energiedosis der Strahlung); die einzelne Strahlendosis beträgt dabei pro Tag 1,8–2 Gy.
Brachytherapie
Alternativ zur externen Bestrahlung kann die Strahlenquelle auch direkt an den Tumor gebracht werden. Bei diesem Brachytherapie genannten Verfahren werden kleine radioaktive Partikel direkt in die Prostata implantiert. Diese Strahlenquellen verbleiben kurzfristig (Afterloading) oder dauerhaft („Seeds“) in der Prostata.
Bei der Seed-Implantation (auch LDR-Brachytherapie: „low-dose-rate“) werden kleinste Strahlungsquellen mit kurzer Strahlung, die sogenannten Seeds (engl.: „Samen“), in die Prostata eingesetzt. Die Platzierung der Seeds erfolgt mit Hilfe von Punktionsnadeln: Unter Ultraschallkontrolle werden die Kurzstrahler an gezielt ausgewählte Stellen der Prostata abgelegt. Die radioaktive Strahlung, die von den Seeds ausgestrahlt wird, zerstört die Krebszellen direkt von innen. Die Platzierung der Seeds dauert etwa zwei Stunden und erfolgt unter einer leichten Vollnarkose oder einer Rückenmarksnarkose. Bei Prostatakrebs im Anfangsstadium ist die Brachytherapie ebenso gut wirksam wie die Bestrahlung von außen; bei einem lokal fortgeschrittenen oder aggressiven Prostatakarzinom wird sie nicht empfohlen.
Beim Afterloading („Nachladeverfahren“, auch HDR-Brachytherapie: „high-dose-rate“) wird eine radioaktive Strahlenquelle über eine Hohlnadel kurzfristig in die Prostata eingebracht. So können zielgenau hohe lokale Dosen (HDR = High-Dose-Rate) verabreicht werden, während gleichzeitig das umgebende Gewebe geschont wird. Diese Form der Behandlung wird derzeit immer mit einer externen Bestrahlung kombiniert.
Wie wirksam ist die Strahlentherapie?
Angaben zur Wirksamkeit der Strahlentherapie sind wegen der unterschiedlichen Dosierungen und Verfahren schwierig. Zudem sind – wie bei der Prostatektomie – die Ergebnisse vom Tumorstadium und anderen Risikofaktoren abhängig. Insgesamt gelten Operation und Bestrahlung aus heutiger Sicht als gleichwertige Verfahren, insbesondere bei frühen Tumoren. In der Praxis sind daher häufig die unterschiedlichen zu erwartenden Nebenwirkungen ein Entscheidungskriterium für die Wahl zwischen Operation und Bestrahlung.
Welche Folgen hat die Strahlentherapie?
Trotz moderner Bestrahlungstechniken sind Beschwerden in Folge der Strahlentherapie möglich, so etwa Entzündungen der Blase und des Darms. Diese Symptome können akut, also während der Therapie, oder kurz danach auftreten, aber es gibt auch Spätfolgen, die erst Monate oder sogar Jahre nach Bestrahlungsende Probleme bereiten.
Auch eine Strahlentherapie hat häufig – bei bis zu 60% der Patienten – Potenzprobleme zur Folge, jedoch seltener als nach einer Operation. Inkontinenz tritt nach einer Bestrahlung seltener auf als nach radikaler Prostatektomie.
Andere lokale Therapieverfahren
Es gibt verschiedene neuere Verfahren, die derzeit getestet werden. Da jedoch noch nicht genügend Ergebnisse vorliegen, werden sie bislang nicht oder nur im Rahmen von Studien empfohlen.
Kryotherapie
Bei der Kryotherapie oder auch Kryochirurgie werden Zellen durch Unterkühlung abgetötet. Dazu platziert der Arzt 12-15 Kryonadeln unter Ultraschall-Kontrolle in der Prostata. Danach werden diese zweimal hintereinander auf -40° C abgekühlt und wieder aufgetaut.
HIFU
Beim Hochintensiven Fokussierten Ultraschall (HIFU) werden unter Narkose hochenergetische Schallwellen über eine im Enddarm platzierte Ultraschallsonde in Richtung Prostata gesendet. Dadurch erhitzt sich das Tumorgewebe auf über 65° C und stirbt ab. Dieses experimentelle Verfahren soll nach den Leitlinien der Deutschen Krebsgesellschaft nur im Rahmen von Studien angewandt werden.
Hormontherapie
Die alleinige Hormontherapie ist keine kurative Behandlung und wird daher bei heilbaren Prostatakarzinomen in der Regel nicht angewendet – es sei denn, die Patienten wünschen es ausdrücklich. Es gibt aber auch Situationen beim lokalen oder lokal fortgeschrittenen Prostatakarzinom, bei denen die Hormontherapie zum Einsatz kommen kann. Dann hat sie das Ziel, den Effekt der kurativen lokalen Therapie zu verbessern:
- Eine zwei- bis dreimonatige (neo-)adjuvante Hormontherapie hat sich bei Patienten mit lokal fortgeschrittenem Prostatakarzinom als vorteilhaft erwiesen, die eine Strahlentherapie erhalten.
- Eine zwei- bis dreijährige adjuvante Hormontherapie ist sinnvoll für Patienten mit lokal fortgeschrittenem Tumor, hohem Progressionsrisiko und/oder Lymphknotenmetastasen nach einer Strahlentherapie.
- Werden Lymphknotenmetastasen entdeckt, kann auch nach radikaler Prostatektomie eine mindestens zweijährige adjuvante Hormontherapie durchgeführt werden.
Die meisten Patienten erhalten eine Hormontherapie jedoch, wenn zum Zeitpunkt der Diagnose bereits Metastasen vorliegen oder wenn ihr Krebs nach einem vorangegangenen kurativen Therapieversuch fortgeschritten ist.
Therapie-Leitlinien
Wie für viele andere Krebsarten gibt es auch für Prostatakrebs verschiedene nationale und internationale Leitlinien, die auf Grundlage der neuesten Forschungsergebnisse entwickelt und regelmäßig aktualisiert werden. Sie helfen den Ärztinnen und Ärzten bei der Entscheidungsfindung in ganz spezifischen Situationen. Die wichtigsten Behandlungsempfehlungen für Prostatakrebs sind:
- S3-Leitlinie der Deutschen Krebsgesellschaft und verschiedener Fachgesellschaften
- Guidelines der Europäischen Gesellschaft für Urologie (EAU)
- Clinical Practice Guidelines des amerikanischen National Comprehensive Cancer Network (NCCN)
Parallel zu diesen Fachpublikationen erscheinen jeweils auch Patientenleitlinien, die in allgemein verständlicher Sprache die aktuellen Empfehlungen wiedergeben.
Quellen:
[1]Prostatakrebs-Leitlinien der European Association of Urology, Stand 2014, http://uroweb.org/guideline/prostate-cancer/
[2]Interdisziplinäre Leitlinie der Qualität S3 zur Früherkennung, Diagnose und Therapie der verschiedenen Stadien des Prostatakarzinoms, Langfassung. Online unter http://leitlinienprogramm-onkologie.de/uploads/tx_sbdownloader/LL_Prostata_Langversion_3.1.pdf
[3] H.-J. Schmoll. K. Höffken, K. Possinger (Hrsg.): Kompendium Internistische Onkologie, Springer Verlag 2006
Fachliche Beratung
Prof. Dr. Kurt Miller
Klinik für Urologie, Charité – Universitätsmedizin Berlin
Prof. Dr. Jürgen Gschwend
Universitätsklinikum rechts der Isar, München